|
I
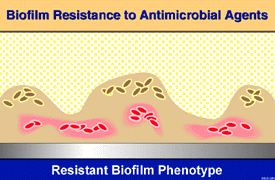
Biofilm contrastano le azioni degli antimicrobici mediante molteplici
meccanismi. Questi si possono ricondurre a tre ampie categorie:
-
Riduzione della concentrazione di antimicrobici nella massa fluida che
circonda il biofilm
-
Inefficacia dell’agente antimicrobico nel penetrare il biofilm
-
Adozione di uno stato di di resistenza fisiologica di almeno una parte
delle cellule del biofilm
Nel
primo caso l’angente antimicrobico è reso inefficace prima di raggiungere il
biofilm. Nel secondo caso, l’agente antimicrobico è trasportato fino alla
superficie del biofilm ma non penetra nello stesso. Nel terzo scenario
l’agente antimicrobico attraversa la superficie del biofilm ma non è in grado
di eliminare i microrganismi in quanto si trovano in uno stato fenotipico che
conferisce loro una ridotta suscettibilità. Di quest’ultimo scenario
distinguiamo due versioni:
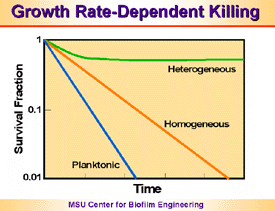
1.
Una carenza di nutrienti porta ad una lenta crescita batterica o a
regioni con ridotta concentrazione di nutrienti nel biofilm.
2.
Presenza di una intrinseca mutazione fenotipica nel biofilm che non
dipende dalla carenza nutrizionale.
Questi meccanismi di
protezione del biofilm non si escludono tra loro., sembra infatti che
combinazioni dei tre tipi di resistenza suddetti lavorino in parallelo.
La
ridotta suscettibilità del biofilm non è stata attribuita agli abituali
meccanismi (mutazione o acquisizione di elementi genetici che attivino una
specifica resistenza genetica) che possano spiegare la resistenza agli
antibiotici convenzionali. In base a questi meccanismi, per spiegare la
resitenza del biofilm, le modificazioni genetiche dovrebbero essere presenti nel
biofilm, ma essere assenti nello stato plactonico. Questo non sembra avvenire
nella generalità dei casi. Sebbene chiaramente suscettibili, i microrganismi,
acquisiscono una marcata resistenza sviluppandosi nel biofilm, infatti, quando
allontanati da un biofilm questi microrganismi tornano rapidamente ad uno stato
di suscettibilità.
1. Deplezione di antimicrobici nella massa fluida
 I I
Se un biofilm esercita una azione di tipo chimico su
un agente antimicrobico con il quale sta interagendo, allora è possibile
ridurre, per queste azioni neutralizzanti, la concentrazione dell’agente nel
fluido. Si consideri ad esempio un test di sensibilità antimicrobica fatto
prima su una sospensione diluita di cellule plankton e poi su biofilm altamente
sporchi. Non è difficile immaginare che la concentrazione di agenti
antimicrobici possa essere mantenuta durante il test con il plankton ma
diminuisca significativamente durante il test con il biofilm. Si potrebbe
argomentare che questo fenomeno non sia dovuto ad un vero e proprio meccanismo
di resistenza ma semplicemente ad un confronto non appropriato. Il biofilm non
è sottoposto alla stessa concentrazione di agenti antimicrobici del test fatto
con il Plankton. Sembra che questo ovvio meccanismo sia stato spesso trascurato.
Potrebbe valere la pena di considerare la diminuzione di agenti antimicrobici
nel fluido come una possibile spiegazione della scarsa performance antimicrobica
sulla pellicola di biofilm. La diminuzione di agenti antimicrobici in un fluido
può essere diagnosticata sperimentalmente misurando le concentrazioni residue
di agenti antimicrobici durante i test sul plankton e sul biofilm. In alcuni
sistemi sperimentali è possibile misurare il potere disinfettante sia sul
plankton che sul biofilm nello stesso fluido, approccio che elimina
elegantemente la possibilità di un trattamento con eguali concentrazioni.
Back to top
2. Transport Limitation of Antimicrobial Penetration
|
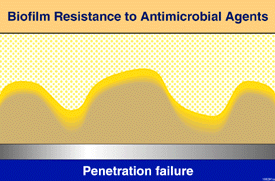
La seconda e più plausibile versione della
limitazione del trasporto di antimicrobici nei biofilm richiede
un’interazione tra l’agente antimicrobico e il biofilm che ne
neutralizza l’attività. La barriera alla penetrazione in questo caso è
reattiva piuttosto che fisica; la percentuale di disattivazione
dell’antimicrobico supera la percentuale di penetrazione di tipo
diffusivo. Questo meccanismo è supportato sperimentalmente in caso di
ipoclorito (de Beer et
al, 1994; Chen and Stewart, 1996; Xu et al, 1996), ed è verosimile essere importante per altri
ossidanti altamente reattivi come l’ozono e l’acqua ossigenata, e può
essere allo stesso modo un fattore per alcuni biocidi non ossidanti(Stewart et al,
1998). É anche realistico per alcuni antibiotici come i
beta-lattami, che sono soggetti ad una rapida degradazione enzimatica.
|
Back to top
| 
 I
I